บทคัดย่อ
เชื้อ
xylose-recombinant Saccharomyces cerevisiae (strain IM2)
ซึ่งมียีน xylose reductase และ xylitol dehydrogenase
แทรกอยู่บนโครโมโซม
สามารถสร้างเอนไซม์ทั้งสองชนิดได้โดยไม่ต้องมีไซโลสเป็นตัวกระตุ้นทำให้ใช้ไซโลสและกลูโคสได้พร้อมกัน
เมื่อเลี้ยง recombinant IM2
ในสภาพที่ให้อากาศด้วยอาหารที่มีน้ำตาลผสมระหว่างไซโลสและกลูโคสความเข้มข้น
3% ในอัตราส่วนต่างๆ (10:0 9:1 7:3 5:5 และ
3:7)พบว่ากลูโคสช่วย
ให้การเจริญของ recombinant IM2
ในไซโลสดีขึ้น และเมื่อศึกษาถึง
อิทธิพลของ pH แหล่งไนโตรเจน
และปริมาณ dissolved oxygen
ที่มีผลต่อการเจริญ
ของ recombinant IM2 เปรียบเทียบกับ Pichia stipitis ซึ่งเป็นยีสต์ที่ใช้ไซโลสได้ดี
ในไฮโดรไลเสทของฟางข้าวซึ่งประกอบด้วยไซโลส
2.5-3.0% และกลูโคส 0.1-0.3% พบว่า recombinant IM2
สามารถเจริญในไฮโดรไลเสทได้ดีกว่า
P. stipitis
Abstract
Xylose-assimilating recombinant Saccharomyces
cerevisiae (strain IM2), constructed by integrating the xylose reductase
and xylitol dehydrogenase genes onto the chromosome produced both enzymes constitutively
and could utilize xylose
together with glucose. Aerobic cultivation of this recombinant in the medium containing 3%
xylose-glucose mixture at various
ratio (10:0, 9:1, 7:3, 5:5 and 3:7) indicated the growth enhancement in the presence of
glucose. Rice straw, one of the abundant
agricultural waste, was hydrolyzed by 1.5% sulfuric acid at 121oC for 30 min
and yielded a mixture of 2.5-3% xylose and 0.1-0.3%
glucose. Effect of N-source, pH, temperature and dissolved oxygen on growth and
fermentation ability of the recombinant IM2
were carried out and compared with P. stipitis, the effective xylose-utilizing
yeast. The results showed that the recombinant IM2
grew in the rice straw hydrolysate better than P. stipitis.
คำนำ
ในแต่ละปีประเทศไทยมีวัสดุเกษตรเหลือใช้มากมาย
เช่น ฟางข้าว ชานอ้อย
และซังข้าวโพด เป็นต้น
หากสามารถนำวัสดุเหล่านี้มาแปรรูปเป็นสารที่มีราคาและ
เป็น ที่ต้องการของอุตสาหกรรม
เช่น การผลิตจุลินทรีย์โปรตีน
การผลิตแอลกอฮอล์เพื่อพลังงาน
นอกจากจะช่วยพัฒนาเศรษฐกิจของประเทศ
ยังช่วยลดมลภาวะได้อีก
ด้วย
วัสดุเกษตรเป็นสารประกอบลิกโนเซลลูโลสและเมื่อย่อยสลายด้วยกรดหรือเอนไซม์จะได้สารผสมของน้ำตาลซึ่งส่วนใหญ่เป็นกลูโคสและไซโลส
แต่เนื่องจาก
Saccharomyces cerevisiae
ไม่สามารถนำไซโลสไปใช้ได้1 จึงมีการนำเทคนิคทางพันธุวิศวกรรมมาประยุกต์ใช้
และสร้าง xylose-assimilating
recombinant S. cerevisiae
ที่สามารถผลิตแอลกอฮอล์จากไซโลสได้2,3
ซึ่งในการศึกษาเบื้องต้นนั้นได้ใช้ไซโลสบริสุทธิ์เป็นแหล่งคาร์บอนดังนั้นในการศึกษา
ครั้งนี้จึงได้ใช้ไฮโดรไลเสทที่ได้จากการย่อยสลายฟางข้าวด้วยกรดเป็นแหล่งคาร์บอนเพื่อศึกษาความเป็นไปได้ในการนำ
recombinant S. cerevisiae IM2
ไปใช้ในการแปรรูปวัสดุเกษตรให้มีประโยชน์สูงสุด
อุปกรณ์และวิธีการ
จุลินทรีย์ที่ใช้ศึกษา:-
Pichia stipitis CBS5773 และ xylose-assimilating recombinant Saccharomyces
cerevisiae IM2 อาหาร
เลี้ยงเชื้อและสภาพการเลี้ยงเชื้อ:-
เลี้ยงเชื้อทั้งสองในอาหาร YPXG (1% yeast
extract, 2% peptone
และน้ำตาลผสมระหว่างไซโลสและกลูโคสความเข้มข้น
3%)
และในไฮโดรไลเสทของฟางข้าวซึ่งบรรจุในฟลาสก์ขนาด
500 มล.อ
โดยปรับสภาพต่างๆเพื่อศึกษาสภาพที่เหมาะสมต่อการเจริญ
ได้แก่ชนิดและปริมาณธาต
ุอาหารเสริม ค่า pH เริ่มต้น
อุณหภูมิ และปริมาณ dissolved oxygen (DO)
แล้วนำไปบ่มใน incubator shaker
ด้วยความเร็ว 200 รอบต่อนาที
เก็บตัวอย่าง
ทุกๆ 24 ชั่วโมง เป็นเวลา 3 วัน
การเตรียมไฮโดรไลเสทของฟางข้าว:-
นำฟางข้าวบดละเอียดมาย่อยสลายด้วยกรดกำมะถัน
1.5%
โดยใช้ฟางข้าวและกรดในอัตราส่วน
1:6 ที่อุณหภูมิ
121oC นาน 30 นาที
กรองด้วยผ้าขาวบางและกระดาษกรองแล้วนำไปปรับ
pH ด้วย 20% NaOH
ผลและวิจารณ์
xylose-assimilating
recombinant Saccharomyces cerevisiae IM2 เป็น recombinant
ที่เกิดจากการชักนำยีนที่เกี่ยวข้องกับ
xylose
metabolism จาก Pichia stipitis คือ xylose reductase และ xylitol
dehydrogenase gene ที่อยู่บนพลาสมิด pEXGD8
เข้าสู่ S. cerevisiae2
และทำให้ยีนทั้งสองแทรกอยู่บนโครโมโซม3
(ภาพที่ 1)
และสามารถสร้างเอนไซม์ทั้งสองชนิดได้โดยไม่ต้องมีไซโลสเป็นตัวกระตุ้น |
|
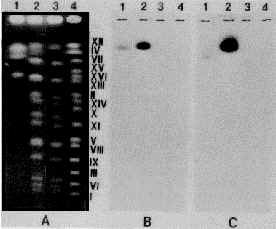
Fig. 1 Site of integration of the
xylose reductase and xylitol dehydrogenase genes in the chromosome of S. cerevisiae. A;
Chromosomes of recombinant IM2, P. stipitis, S. cerevisiae TJ1 as a host strain and
SH964 as a standard marker were separated by CHEF-electrophoresis. Numbers on the right
side indicate chromosome numbers. B and C; The autoradiograms of the hybridization bands
specific to the probes of the xylose reductase and xylitol dehydrogenase genes,
respectively. In each panel, lane 1, 2, 3 and 4 represent the chromosomes (A) or
hybridization bands (B and C) of P. stipitis, IM2, TJ1 and SH964, respectively.
|
|
|
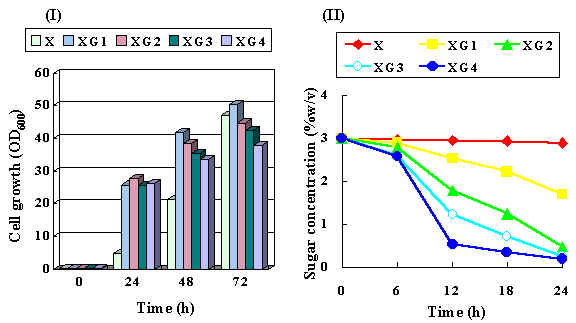
Fig. 2 Growth (I) of
the recombinant IM2 and sugar remained (II) in YPXG medium containing 3% of xylose and
glucose
mixtures at
various ratios; X = 10:0, XG1 = 9:1, XG2 = 7:3, XG3 = 5:5 and XG4 = 3:7 |
เมื่อเลี้ยง
recombinant IM2 ในอาหาร YPXG
ที่มีน้ำตาลผสมระหว่างไซโลสและกลูโคสความเข้มข้น
3% ในอัตราส่วนต่างๆ คือ 10:0 9:1 7:3 5:5
และ 3:7 ในสภาพที่ให้อากาศ พบว่า
recombinant IM2
เจริญในอาหารที่มีไซโลสและกลูโคสได้ดีกว่าอาหารที่มีไซโลสเพียงอย่างเดียวและสามารถใช้น้ำตาล
ได้เร็วขึ้นโดยเฉพาะใน 24
ชั่วโมงแรก (ภาพที่ 2) แสดงว่า
กลูโคสมีส่วนช่วยให้การเจริญของ
recombinant IM2 ในไซโลสดีขึ้น
ซึ่งต่างไปจาก xylose-
assimilating yeast
ปกติที่กลูโคสจะมีผลชลอการไซโลสไปใช้4,5
ดังนั้นไฮโดรไลเสทของวัสดุเกษตร
เช่น ฟางข้าวที่มีไซโลส 2.5-3.0% และ
กลูโคส 0.1-0.3% เป็นองค์ประกอบ
จึงเป็นวัตถุดิบที่สามารถนำไปใช้เลี้ยง
recombinant IM2 ได้
และเมื่อทดลองหาสภาพที่เหมาะสมในการเจริญของ
recombinant IM2 โดยเปรียบเทียบกับ P. stipitis ได้ผลดังนี้
ชนิดและปริมาณธาตุอาหาร
การเติมธาตุอาหารเสริมสามารถเพิ่มการเจริญของ
recombinant IM2 และ P. stipitis
ได้โดยธาตุอาหารเสริมสูตรที่ 2
คือ 0.2% urea 0.3% KH2PO4 และ 0.025% MgSO4.7H2O
จะทำให้เชื้อทั้งสองมีการเจริญสูงสุดในเวลา
3 วัน (ภาพที่ 3)
|
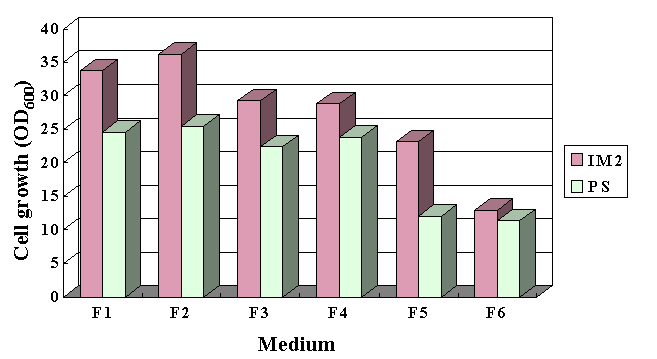
Fig.
3 Cell growth of recombinant IM2 and P. stipitis in supplementedrice straw
hydrolysate
F1; 0.1%
urea, 0.3% KH2PO4 and 0.025% MgSO4.7H2O
F2; 0.2%
urea, 0.3% KH2PO4 and 0.025% MgSO4 .7H2O
F3; 0.4%
urea, 0.3% KH2PO4 and 0.025% MgSO4 .7H2O
F4; 0.1%
yeast extract, 0.1% urea, 0.3% KH2PO4 and 0.025% MgSO4 .7H2O
F5; 0.4%
yeast extract, 0.47% (NH4)2SO4, 0.11% KH2PO4,
0.05% Na2HPO4, and 0.05% MgSO4 .7H2O
F6; no
supplement added |
pH เริ่มต้น
recombinant IM2
เจริญได้ดีในไฮโดรไลเสทที่มี pH
เริ่มต้นระหว่าง 4.0-7.0 ในขณะที่ P.
stipitis เจริญได้ในไฮโดรไลเสทที่มี
pH
เริ่มต้นระหว่าง 5.0-7.0
แต่อย่างไรก็ตามเมื่อเลี้ยงเชื้อทั้งสองชนิดในอาหาร
YPXG ที่มี pH
เริ่มต้นเช่นเดียวกับในไฮโดรไลเสทพบว่าเชื้อทั้งสองชนิดนั้นเจริญได้ดี
ในทุก pH (ภาพที่ 4)
แสดงให้เห็นว่าสารที่ยับยั้งการเจริญของ
P. stipitis น่าจะเป็น inhibitor
อื่นในไฮโดรไลเสทและการปรับ pH
ให้เป็นกลางมากขึ้นจะช่วยลด
ความเป็นพิษของ inhibitor ที่มีต่อ P.
stipitis นอกจากนี้ยังแสดงว่า recombinant IM2
ทนต่อ inhibitor ต่างๆได้ดีกว่า P. stipitis
และจากการทดสอบยืนยัน
ด้วย acetic acid ซึ่งเป็น inhibitor
ชนิดหนึ่งที่พบใน hydrolysate6,7 พบว่า
recombinant IM2 ทนต่อ 0.5 % acetic acid ได้ ส่วน P. stipitis
ไม่สามารถเจริญในอาหารที่มี acetic acid
|
|
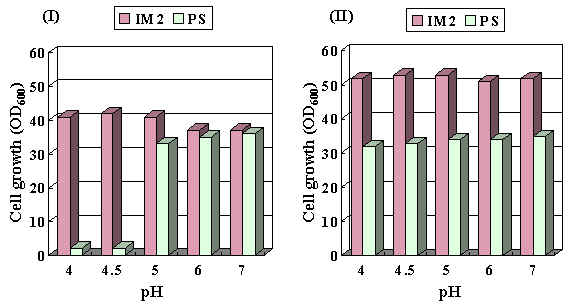
Fig. 4 Effect of pH
on growth of recombinant IM2 and P. stipitis in rice hydrolysate (I) and YPXG
medium (II)
|
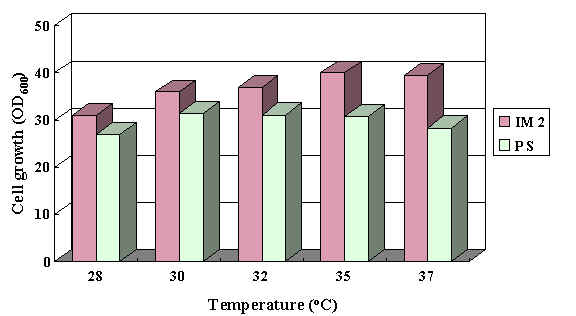
อณหภูมิ
recombinant IM2 และ P. stipitis
เจิรญได้ในช่วงอุณหภูมิ 28-37oC
โดย recombinant IM2
มีแนวโน้มทนต่ออุณหภูมิสูงได้ดีกว่า
P. stipitis (ภาพที่ 5)
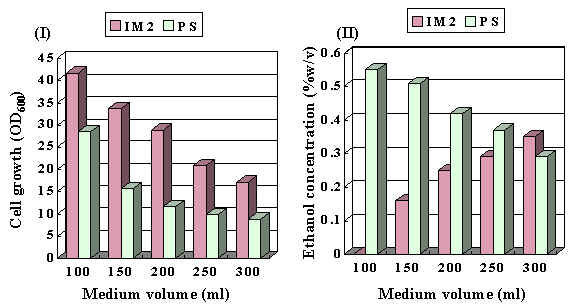
ปริมาณ
dissolved oxygen recombinant IM2 และ P. stipitis
มีการเจริญสูงสุดเมื่อเลี้ยงในไฮโดรไลเสทปริมาตร
100 มล.ซึ่งบรรจุอยู่ในฟลาสก์
ขนาด 500 มล.
และการเจริญจะลดลงเมื่อ
ปริมาตรของไฮโดรไลเสทเพิ่มขึ้นมีผลให้ปริมาณ
DO ลดลง
แต่ถ้าพิจารณาถึงการผลิตแอลกอฮอล์
พบว่า recombinant
IM2
จะสร้างแอลกอฮอล์เพิ่มขึ้นเมื่อปริมาณ
DO ลดลง ส่วน P. stipitis นั้นต้องการ oxygen
ทั้งเพื่อการเจริญและการสร้างแอลกอฮอล์
(ภาพที่ 6) ทั้งนี้เป็นผลมาจาก
custer effect
ที่เกิดขึ้นในสภาพที่มีอากาศจำกัด8
ดังนั้น oxygen
จึงเป็นตัวแปรที่สำคัญที่ใช้ในการควบคุมการผลิตเพื่อให้การเจริญและผลิตแอลกอฮอล์จากไซโลส
ของ recombinant IM2 และ P. stipitis
เป็นไปอย่างเหมาะสมและมีประสิทธิภาพสูงสุด
|
|
Fig. 5
Effect of temperature on growth of recombinant IM2 and P. stipitis |
|
Fig. 6 Effect of medium volume on
cell growth (I) and ethanol production (II) of recombinant IM2 and
P. stipitis
in rice straw hydrolysate
|
จากผลการทดลองนี้สรุปได้ว่า
recombinant IM2
เจริญได้ดีในอาหารเลี้ยงเชื้อที่มีไซโลสและกลูโคสเป็นแหล่งคาร์บอนและเจริญในไฮโดรไลเสท
ของฟางข้าวได้ดีกว่า P. stipitis
และมีการเจริญสูงสุดในไฮโดรไลเสทที่เติม
0.2% urea 0.3% KH2PO4 และ 0.025% MgSO4.7H2O
เป็นธาตุอาหาร
เสริม ปรับ pH เริ่มต้นระหว่าง 4-7
ปริมาตร 100 มล. บรรจุในฟลาสก์ขนาด 500
มล. แล้วนำไปบ่มใน incubator shaker อุณหภูมิ
30-35oC ที่ความเร็ว
200 รอบต่อนาที เป็นเวลา 3 วัน
และมีปริมาณ dissolved oxygen
เป็นปัจจัยสำคัญในการควบคุมขบวนการหมักแอลกอฮอล์ของ
recombinant IM2
เอกสารอ้างอิง
1. Batt, C. A., S. Carvallo, Jr. D. D. Easson, M. Akedo and A. J. Sinsky. 1986.
Biotechnol. Bioeng. 28:549-553.
2. Tantirungkij, M., N. Nakashima, T. Seki and T. Yoshida. 1993. J. Ferment. Bioeng.
75:83-88.
3. Tantirungkij, M., I. Tamaki, T. Seki and T. Yoshida. 1994. Appl. Microbiol. Biotechnol.
41:8-12.
4. Panchal, C. J., L. Bast, I. Russel and G. G. Stewart. 1988. Can. J. Microbiol.
34:1316-1320.
5. Grootjen, D. R. J., M. L. Jensen, R. G. J. M. van der Lans and K. Ch. A. M. Luyben.
1991. Enzyme Microb. Technol.
13:828-833.
6. Vanzyl, C., B. A. Prior and J. C. du Preez. 1988. Appl. Biochem. Biotechnol.
17:357-369.
7.. . 1991. Enzyme Microb. Technol. 13:82-86.
8. Laplace, J. M., J. P. Delgenes, R. Moletta and J. M. Navarro. 1991. Appl. Microbiol.
Biotechnol. 36:158-162.
|
|

